Neste Blog realizamos: 1 - Atualização sobre SAÚDE PÚBLICA, PESQUISA BIOMÉDICA E BIOSSEGURANÇA. 2 - Atualização sobre a ocorrência de Doenças de importância em animais de laboratório e outras espécies. 3 - Troca de Informações sobre Doenças Infecciosas, Zoonoses, Licenciamento Ambiental, Defesa Sanitária Animal, Vigilância Sanitária, Boas Práticas de Laboratório e demais assuntos relacionados à sanidade e Saúde Pública.
Pesquisar Neste Blog
sexta-feira, 18 de março de 2011
Agenda Fiocruz - Março 2011 21/03 a 26/03
I Seminário sobre gestão e curadoria de coleções zoológicas da Fiocruz.
Inscrições de 2 a 11/3: 25 vagas.
Horário: 8h15
Local: auditório Emmanuel Dias / Pavilhão Arthur Neiva / IOC
O evento ocorre até o dia 25/3.
Defesa de dissertação de mestrado profissionalizante em saúde pública na Ensp: Diagnóstico situacional das doenças relacionadas ao trabalho em profissionais de enfermagem do Hospital de Base Dr. Ary Pinheiro/Porto Velho. Por Tatiana Tomoe Do Martins. Orientadora: Rejane Corrêa Marques.
Horário: 9h
Local: sala de aula da Unir
TERÇA-FEIRA: 22/3
Defesa de dissertação de mestrado em saúde pública na Ensp: Estudo sobre o processo de medicalização de crianças no campo da saúde mental em um serviço de atenção básica no município do Rio de Janeiro. Por Valéria Nogueira Leal Sanches. Orientador: Paulo Duarte de Carvalho Amarante.
Horário: 9h30
Local: sala 410 da Ensp
Defesa de dissertação de mestrado em biologia parasitária no IOC: Avaliação de diferentes coletores de fluido oral para detecção da resposta imune humoral contra o vírus da hepatite A e sua aplicação em estudo epidemológico em áreas de dificil acesso. Por Renata Tourinho Santos. Orientadora: Vanessa Salete de Paula.
Horário: 10h
Local: auditório Maria Deane / Pavilhão Leônidas Deane / IOC
QUARTA-FEIRA: 23/3
Seminário internacional na COC: Relações médico-científicas entre Brasil e Alemanha – história e perspectivas.
Horário: 9h
Local: auditório do Museu da Vida
O evento continua até 25/3.
Palestra internacional na Ensp: O cenário epidemiológico das micro bactérias não tuberculosas (MNTB) nos Estados Unidos. Por Rebecca Prevots, responsável pela unidade epidemiológica do National Institute of Health (NIH).
Horário: 11h
Local: auditório do Centro de Referência Prof. Hélio Fraga / Ensp
Defesa de dissertação de mestrado profissionalizante em saúde pública na Ensp: Caracterização epidemiológica da Leishmaniose Tegumentar Americana no município de Rio Branco-Acre no período de 2000 a 2008. Por Ana Cristina Miranda de Oliveira. Orientador: Valmir Laurentino Silva.
Horário: 13h
Local: sala 24 do DCB / Ensp
Centro de estudos da Ensp: exibição do documentário Positivas seguido de debate com a diretora Susanna Lira, mediado pela pesquisadora Angela Escher, da Ensp.
Horário: 14h
Local: Salão Internacional da Ensp
QUINTA-FEIRA: 24/3
Encontro às quintas na COC: O Alufá Rufino – tráfico, escravidão e liberdade no Atlântico Negro. Por João José Reis, da UFBA, e Flávio dos Santos Gomes, da UFRJ.
Horário: 10h
Local: sala 407 do Prédio da Expansão
SEXTA-FEIRA: 25/3
Centro de estudos do IOC: Coleções biológicas da Fiocruz – reconhecimento e expectativa institucionais. Por Claude Pirmez, vice-presidente de Pesquisa e Laboratórios de Referência da Fiocruz – evento integrado ao I Seminário sobre gestão e curadoria de coleções zoológicas da Fiocruz.
Horário: 10h
Local: auditório Emmanuel Dias / Pavilhão Arthur Neiva / IOC
SÁBADO: 26/3
Encontro Mulher Manguinhos da Ensp.
Horário: 13h
Local: Colégio Estadual Compositor Luiz Carlos da Vila
Novo biofármaco pode aprimorar o tratamento do diabetes
Um biofármaco que acaba de ser desenvolvido por pesquisadores da Universidade Federal do Rio de Janeiro (UFRJ) – e que já teve seu pedido de patente depositado no Instituto Nacional da Propriedade Industrial (INPI) – pode representar um novo caminho para tornar o tratamento do diabetes mais eficaz. O medicamento, produzido no Laboratório de Biotecnologia Farmacêutica da universidade (BiotecFar), é baseado em um sistema de liberação prolongada de amilina humana e tem como objetivo oferecer aos diabéticos um melhor controle da glicemia. Trocando em miúdos, a amilina é um hormônio produzido naturalmente no pâncreas (pelas células beta), que desempenha um papel fundamental em diversos órgãos, inclusive para equilibrar os níveis de glicose. Este hormônio é cosecretado com a insulina, exercendo conjuntamente papéis importantes na regulação metabólica. "Mesmo pacientes diabéticos que fazem uso da insulina possuem dificuldades de controle dos níveis de glicose no sangue", explica o professor da UFRJ Luís Maurício Lima, coordenador do projeto que teve início em 2009. Atualmente, o tratamento para diabetes leva em conta apenas a reposição de insulina, deixando de lado a reposição da amilina. Isso ocorre devido à dificuldade de desenvolver medicamentos a base de amilina humana, que é bastante insolúvel. "Ao contrário da insulina, que é livremente solúvel, a amilina humana tem um problema de agregação protéica, que inclusive é causa de diabetes amiloidogênica e ainda a razão da dificuldade de usar o hormônio natural terapeuticamente", afirma o farmacêutico. Para contornar esse obstáculo e desenvolver o novo medicamento, os pesquisadores do BiotecFar/UFRJ recorreram a um minucioso trabalho de nanobiotecnologia farmacêutica. No laboratório, eles encapsularam nanopartículas de amilina humana em partículas poliméricas biocompatíveis. Por serem tão pequenas, elas podem ser facilmente administradas por injeção subcutânea ou intramuscular e por terem como base polímeros biocompatíveis são naturalmente degradadas e eliminadas pelo organismos. Apesar de continuarem insolúveis, formam um depósito que vai se degradando aos poucos no local de aplicação. "Produzimos nanopartículas contendo amilina humana de 200 nanômetros, que é uma medida equivalente a cerca de um milionésimo de metro", conta Lima. | ||||
Uma vantagem do uso de nanopartículas é a liberação contínua e lenta da amilina humana. Esta característica permite que as aplicações de amilina humana, sejam por injeções intramuscular ou subcutânea, não precisem ser diárias. "Esse detalhe é importante para manter a qualidade de vida do paciente diabético que já recebe doses diárias de insulina. Assim, o paciente não precisaria receber mais injeções diárias, de análogos solúveis de amilina, o que tornaria o tratamento mais desconfortável e menos próximo ao fisiológico por não se tratar da amilina humana. Podemos programar aplicações semanais ou até mensais", destaca o professor. "A ideia é que a reposição de amilina humana seja um tratamento complementar à reposição de insulina, para potencializar o controle da glicemia", completa. O medicamento desenvolvido pelo projeto, que contou com apoio da FAPERJ por meio dos editais Jovem Cientista do Nosso Estado e Apoio às Instituições de Ensino e Pesquisa Sediadas no Estado do Rio de Janeiro, é uma alternativa ao uso de outro medicamento disponível no mercado americano para reposição da amilina: o pramlintide. "A diferença é que o pramlintide não é encontrado naturalmente no corpo e, por isso, pode causar alguns efeitos colaterais indesejados. Ele é uma substância análoga da amilina humana com alguns aminoácidos modificados para se tornar solúvel. Já a proposta da nossa equipe é oferecer um medicamento totalmente biocompatível", pondera Lima. Apesar do sucesso dos testes de controle de glicemia em camundongos, realizados no Laboratório de Biotecnologia Farmacêutica da universidade, ainda não há previsão de quando será possível viabilizar a chegada da amilina humana ao mercado. "Estamos em busca de parcerias com indústrias farmacêuticas e agências de fomento para realizar testes clínicos em humanos e, posteriormente, inserir o novo medicamento no mercado", conclui. Além do professor Luís Maurício Lima, fazem parte da equipe o doutorando do Programa de Pós-graduação em Ciências Farmacêuticas Luiz Henrique Guerreiro e os professores da Faculdade de Farmácia Eduardo Ricci e Mauro Sola Penna. Sobre o diabetes O diabetes é uma doença metabólica caracterizada pela redução da quantidade de insulina secretada pelo pâncreas ou pela diminuição da sensibilidade do organismo à ação da insulina, o que eleva a quantidade de açúcar no sangue (hiperglicemia). Ele já é considerado uma epidemia associada à obesidade. De acordo com estatística divulgada pela Sociedade Brasileira de Diabetes (SBD), um novo caso surge a cada cinco segundos no mundo. Cerca de 250 milhões de pessoas em todos os países tem diabetes e a projeção feita pela Organização Mundial de Saúde (OMS) para o ano de 2030 é que esse número dobre. No Brasil, segundo a SBD, pelo menos 10 milhões de pessoas têm a doença – o equivalente a 5,9% da população brasileira. |
Uenf disponibiliza diagnóstico rápido para doenças genéticas
 |
| Para Medina-Acosta, uma das grandes vantagens do novo teste é a rapidez com que fornece os resultados |
Comprimido magnético controla absorção de medicamentos
 |
| O comprimido magnético poderá ser útil em vários casos, incluindo os pacientes com diabetes ou câncer e na pesquisa de novos medicamentos. |
Microssensor detecta lesões que antecedem a aterosclerose
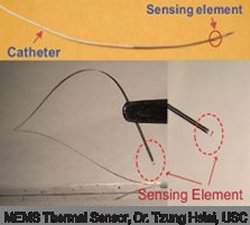 |
| O novo sensor foi construído a partir de uma pastilha feita com titânio e platina aplicados sobre plástico. |
Stem Cells May Be Key to Understanding the Origins of Colon Cancer and Detecting Relapse
 |
Intestinal epithelium with tumour stem cells marked in brown. |

%20e%20doutorandoluiz%20henriqueguerreiro_credito_bruno%20melo%20ferreira_peq.jpg)

