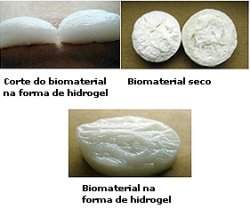
 |
| O hidrogel pode ser preparado de diversas maneiras, de acordo com a função a que se destina. |
A solução para o preenchimento de defeito ósseo, especialmente o da região da face, pode estar em um hidrogel à base de biomateriais como a quitosana e a hidroxiapatita.
O hidrogel mistura um teor de componente inorgânico (a hidroxiapatita) e um teor de componente orgânico (a quitosana) similares aos encontrados no osso humano, no qual o componente orgânico corresponde a diversas proteínas, majoritariamente colágeno.
A inovação é fruto do trabalho de Geovanna Pires e Valéria Pagotto Yoshida, do Instituto de Química da Unicamp.
Hidrogel
O hidrogel pode ser preparado de diversas maneiras, desde a forma de um gel úmido, com resistência suficiente para ser manipulado e fracionado em um eventual implante ou para a realização de preenchimento de defeito ósseo, sendo que nesse caso ele pode ser preparado como um material esponjoso e rígido.
Por ser manipulável, é um forte candidato ao preenchimento. "Temos portanto um material nas duas formas", descreve Yoshida.
Ele também pode ser preparado na forma de um xerogel, ou seja, um gel seco, poroso, com estrutura bem-definida, que poderia ser utilizado como arcabouço para processos de engenharia de tecidos.
Após a obtenção do hidrogel, ele é cortado pelo cirurgião - médico ou dentista - no mesmo formato da falha óssea, como a de uma fratura, por exemplo, com o objetivo de preenchê-la. A peça então preparada assumiria a forma exata para que pudesse ser devidamente implantada no local.
A pesquisadora revela que a aparência do hidrogel lembra a de uma cartilagem, enquanto intumescido em solução de fluido corpóreo ou em solução que pode conter medicamentos importantes no momento do implante, capaz de atuar como matriz temporária para auxiliar na proliferação celular e na deposição da matriz extracelular, para a troca progressiva do biomaterial por uma estrutura regenerada e reconstituída.
Quando seco, parece um osso. Mas é diferente dos materiais atuais, que já são encontrados em pedaços sólidos e não moldáveis, os quais, quando usados para o preenchimento de falhas ósseas, precisam completar os seus vazios com uma pasta auxiliar. O gel do estudo desponta como um material único, que elimina totalmente a necessidade dessa pasta.
Geovanna Pires explica que a durabilidade do hidrogel ainda não está esclarecida, o que demandaria testes in vivo. No trabalho, a pesquisadora fez os testes apenas in vitro. Isso porque, enquanto era desenvolvido o produto, salienta Yoshida, ocorreu uma mudança na legislação dos biotérios e, por isso, houve grande dificuldade de acesso a animais para levar adiante esta etapa.
Quitosana e hidroxiapatita
O material forma um hidrogel moldável constituído de quitosana e de hidroxiapatita nucleada que cresce in situ. Enquanto intumescido, ou ainda na forma de xerogel (seco), com uma estrutura rígida muito semelhante à encontrada em osso desproteinado (poroso), apresenta uma série de poros interconectados, que vão desde macroporos até microporos semelhantes ao osso, proporcionando a difusão de nutrientes para os tecidos.
Além disso, na presença de silício (não silício elementar, e sim siloxano), a fase de hidroxiapatita nucleia mais rapidamente e em maior quantidade, confirmando assim algumas suspeitas descritas na literatura de que o silício é um componente valiosíssimo na nucleação da fase inorgânica do osso.
Algumas vantagens ainda associadas aos biomateriais aqui avaliados estão na sua preparação, que acaba não gerando resíduos de fabricação e eles se sobressaem entre outros pela facilidade na fase de moldagem. "Isso poderia ser feito in loco no ato cirúrgico", sugere Bertran.
Geovanna Pires garante que há muitas patentes envolvendo hidroxiapatita e os demais componentes orgânicos. Contudo, a sua tarefa foi um pouco além: "desenvolvemos um processo de obtenção diferente, uma vez que a grande maioria deles relaciona-se a pastas, misturando-se hidroxiapatita em pó, por processo mecânico, a uma fase orgânica, das mais diferentes formas, porém sem o controle da estrutura", completa.
Controle de porosidade
Materiais com controle de porosidade, prossegue a pesquisadora, é um dos pré-requisitos para o sucesso da implantação e da regeneração de tecidos ósseos. Deste modo, quanto mais se assemelhar ao osso, mais este material terá a chance de ser bem-sucedido.
"A propósito, procuram-se em geral componentes com estrutura que mais se aproxime do colágeno e da hidroxiapatita", comenta Yoshida. O novo hidrogel conseguiu parecer mais com o osso do que os produtos similares disponíveis no mercado.
Um aspecto bastante curioso da pesquisa na formação da parte inorgânica do hidrogel é que, de certa forma, ele está mimetizando aquilo que certamente acontece na formação do osso.
"No organismo, a hidroxiapatita nucleia e cresce em uma matriz orgânica constituída majoritariamente de colágeno, que é mais ou menos o que acontece na formação do hidrogel, no qual a hidroxiapatita nucleia e cresce em uma matriz de quitosana. Essa é a grande diferença de uma 'pasta mecânica' composta de um pó de hidroxiapatita e de outra fase orgânica", esclarece Yoshida.
Mercado
Geovanna conta que o produto deve agora ser levado à escala piloto e, em seguida, à escala industrial.
Mas o primeiro passo nesta direção já foi dado pela especialista ao entrar com um pedido de depósito de patente junto ao Instituto Nacional da Propriedade Intelectual (Inpi), já concedido em 2010.
"As indústrias mais interessadas no produto seriam as de biomateriais e as especializadas em preenchimento ósseo na área odontomédica", informa.
Segundo Yoshida, um dos objetivos da investigação foi o estudo de nucleação e crescimento de partículas de hidroxiapatita sobre um material que simulasse o colágeno, comparando-se a nucleação e o crescimento das partículas da fase inorgânica na presença e na ausência de siloxanos solúveis (família de substâncias químicas que são derivadas do silício).
A nucleação corresponde a um processo no qual moléculas ou íons dispersos na solução se aglomeram em escala nanométrica. Estes aglomerados constituem o núcleo e apenas se tornam estáveis a partir de um certo tamanho crítico, que depende das condições nas quais a nucleação ocorre. É durante este processo que os íons ou moléculas se arranjam de uma forma definida e periódica, determinando a estrutura do cristal.
Segundo a pesquisadora, existem poucos trabalhos na literatura que se referem ao valor do silício solúvel na nucleação da fase inorgânica do osso, apesar de hoje haver um consenso sobre a importância deste elemento no organismo. "Nós nos propusemos a estudar o efeito do silício, sob a forma de siloxano, na nucleação da fase de hidroxiapatita, em presença do material orgânico", afirma.
O uso da quitosana como biomaterial é bastante difundido, contudo pouco foi esclarecido acerca do seu emprego na formação da hidroxiapatita in situ.
Neste sentido, a linha de pesquisa de Yoshida procurou conjugar o seu conhecimento no assunto relativo ao comportamento dos siloxanos, introduzindo-os nos processos que levam à nucleação e ao crescimento in situ das partículas de hidroxiapatia, por haver fortes indícios de que tal elemento químico, pertencente ao grupo do carbono, é também decisivo neste processo.
A intenção de Geovanna Pires foi a de tentar estabelecer os fatos que levam à nucleação de hidroxiapatita e à incorporação de siloxano neste material.



1740-8261/asset/VRU_centre.gif?v=1&s=7740c7f96f65ef3c70d866e72e2a79e7ebe9c5de)
